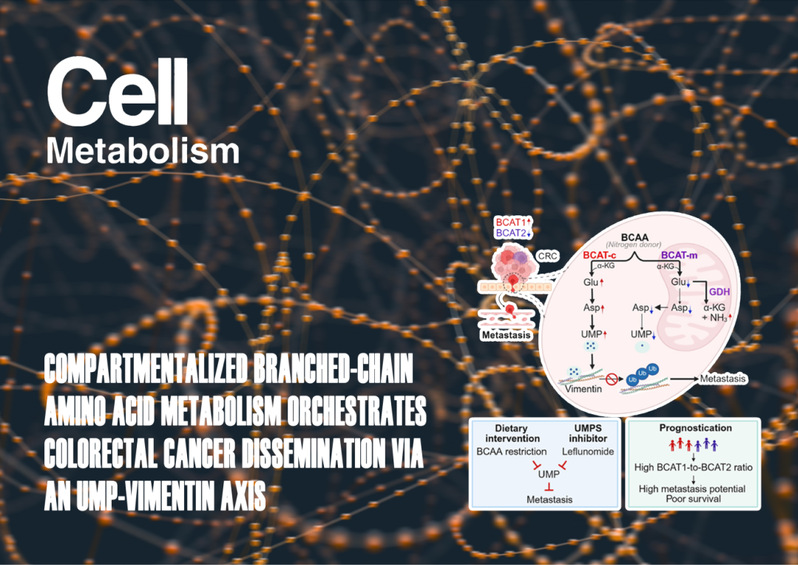
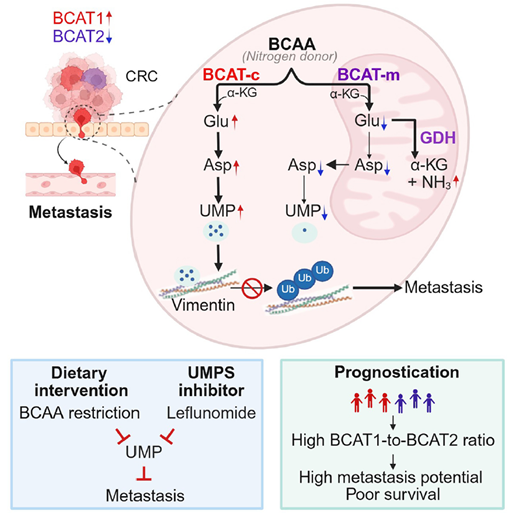
质谱分析的基础理论及其在生命科学,环境毒理以及药物开发的应用研究;目前主要研究与环境新污染物和食品安全相关的人体健康和疾病。
背景介绍
1982年在厦门大学获得化学学士学位,1990年在德国University of Marburg获得分析化学博士学位,1991-2000年分别在美国的Nebraska 大学和Glaxo-Wellcome药物公司工作,2001年起受聘于香港浸会大学,郭一苇讲座教授,环境与生物分析国家重点实验室主任和二恶英实验室主任。
蔡教授2003年获得国家“杰出青年”(海外);2013年获得国家级人才;2021年当选英国皇家化学学会会士(FRSC);2023年欧洲科学院院士(MAE),2024年中国化学会会士(FCCS);曾获教育部高等学校科学研究优秀成果奖自然科学奖二等奖(2018);中国分析测试协会科学技术奖特等奖(2020)和国家自然科学二等奖(排名第五,2011)。
研究领域
质谱分析的基础理论及其在生命科学,环境毒理以及药物开发的应用研究;目前主要研究与环境新污染物和食品安全相关的人体健康和疾病。
教育背景
1987.9-1990.10,博士(分析化学),德国马尔堡大学化学系
1978.9-1982.6,学士(分析化学),厦门大学
工作经历
2024.07 - 至今,宁波东方理工大学讲席教授
2015 – 2024,香港浸会大学化学系,郭一苇环境与生物分析教授
2013 – 2024,环境与生物分析国家重点实验室(香港浸会大学)主任
2010 – 2024, 香港浸会大学化学系,化学讲座教授
2003 – 2024,香港浸会大学二恶英分析实验室主任
2012 – 2015,香港浸会大学研究生院,副院长
2007 – 2011, 香港浸会大学化学系,系主任
2006 – 2010, 香港浸会大学化学系,教授
2001 – 2005,香港浸会大学化学系,副教授
1997 - 2000,美国Glaxo-Welcome药物公司,研究员
1994 – 1996,美国University of Nebraska-Lincoln, 研究助理教授
学术兼职(部分)
2013 – 至今,Rapid Communication in Mass Spectrometry (Wiley),Editor
2021 – 至今,Environmental Science: Advances (RSC),co-Editor in Chief
2021 – 至今,环境化学,副主编
2023 – 至今,National Science Review(Chemistry)编委,
2020 – 2023,The Innovation,编委
2023 – 至今,The Innovation Life Science,编委
2019 – 至今,国家食品安全风险评估中心,外聘学科带头人
2015 – 至今,香港食品安全专家委员会成员
2011– 至今,中国毒理学会分析毒理分会委员
2010– 至今,中国化学会有机分析分会委员
2010 – 至今,中国化学会环境化学分会委员
2008 – 至今,中国环境科学学会环境化学分会委员
2004 – 至今,中国色谱学会理事
2004 – 至今,中国质谱学会理事
获奖情况及荣誉
2024,中国化学会会士(FCCS)
2023,欧洲科学院院士 (MAE)
2021,英国皇家化学会会士 (FRSC)
2020,中国分析测试协会科学技术奖特等奖
2019,全球“分析科学家”
教育部高等学校科学研究优秀成果奖
2016,中国分析测试协会科学技术奖一等奖
2011,国家自然科学二等奖(排名第五)
以通讯作者或者共同通讯作者在Nature Communications, Nature Protocols, Proceedings of the National Academy of Science(PNAS), The Innovation,和Science Bulletin 等杂志上发表SCI论文800多篇,他引次数30000次以上,H影响因子82(Scopus)。
论著信息及引用数据
Scopus
https://www.scopus.com/authid/detail.uri?authorId=7402904946
Web of science (Clarivate)
https://www.webofscience.com/wos/author/record/ABD-4001-2020
10篇代表作(*表示通讯作者)
1. Xu H, Jiang T, Lin Y, Zhang L, Yang H, Huang X, Mao R, Yang Z, Zeng C, Zhao S, Di L, Zhang W, Zeng J*, Cai Z*, Lin SH*, LipidIN: a comprehensive repository for flash platform-independent annotation and reverse lipidomics. Nature Communications, 2025, 16(1): 1-17.
2. Song Y, Zhang Y, Zhu L, Chen Y-Y, Chen Y-J, Zhu Z, Feng J, Qi Z, Yu J, Yang Z*, Cai Z*, Phosphocholine-induced energy source shift alleviates mitochondrial dysfunction in lung cells caused by geo-specific PM2.5 components, PNAS, 2024, 121(14), e2317574121.
3. Zhang J, Walker ME, Sanidad KZ, Zhang H, Liang Y, Zhao E, Chacon-Vargas K, Yeliseyev V, Parsonnet J, Haggerty TD, Cai Z*, Redinbo MR*, Zhang G*, Microbial enzymes induce colitis by reactivating triclosan in the mouse gastrointestinal tract, Nature communications, 2022, 13(1): 136.
4. Xiao C, Li K, Hua J, He Z, Zhang F, Li Q, Zhang H, Yang L, Pan S, Cai Z*, ZL Yu, KB Wong, Xia YJ*, Arabidopsis DXO1 activates RNMT1 to methylate the mRNA guanosine cap., Nature Communications, 2023, 14(1): 202.
5. Yang Z, Wu D, Lu S, Qiu Y, Hua Z, Tan F, Zhang C, Zhang L, Zhang D-Y, Zhou X*, Cai Z*, Shang Y*, Lin SH*, Plasma Metabolome and Cytokine Profile Reveal Glycylproline Modulating Antibody Fading in Convalescent COVID-19 Patients, PNAS, 2022, 119(34): e2117089119.
6. Zhao C, Guo L, Dong J*, Cai Z*, Mass spectrometry imaging-based multi-modal technique: Next-generation of biochemical analysis strategy, The Innovation, 2021, 2(4): 100151.
7. Zhao C, Xie PS, Yong T, Huang W, Liu JJ, Wu DS, Ji FF, Li M, Zhang DD, Li RJ, Dong C, Ma J, Dong Z, Liu SJ, Cai Z*, Airborne fine particulate matter induces cognitive and emotional disorders in offspring mice exposed during pregnancy, Science Bulletin, 2021, 66(6): 578-591.
8. Luan HM, Zhao HZ, Li JF, Zhou YQ, Fang J, Liu HX, Li YY, Xia W, Xu SQ*, Cai Z*, Machine learning for investigation on endocrine-disrupting chemicals with gestational age and delivery time in a longitudinal cohort, Research, 2021,2021: 9873135.
9. Zhang HL, Zhong H, Wang XF, Zhang SD, Shao XJ, Hu H, Yu ZL, Cai Z*, Chen XM*, Xia YJ*, Use of NAD tagSeq II to identify growth phase-dependent alterations in E coli RNA NAD+ capping, PNAS, 2021, 118(14): e2026183118.
10. Shao XJ, Zhang HL, Yang Z, Zhong H, Xia YJ*, Cai Z*, NAD tagSeq for transcriptome-wide identification and characterization of NAD+-capped RNAs, Nature Protocols, 2020, 15(9): 2813-2836.
本科生课程:
1.大学化学
课题组现有成员19人,包括:
•研究助理教授:苏秀丽、王玮敏
•博士后:贺圆珍、闫凌、郗乐怡、孙倩倩
•博士研究生:罗伟强、谷瑞楠、柳安萍、洪志龙、罗伊君、武海江
•科研助理:黄宇涵、朱子凡、田心仪、李萍、常维夏、汪慧明
•实习生:张一诺